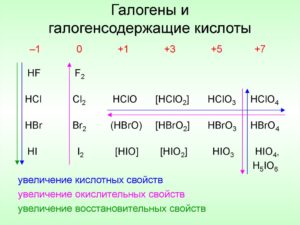
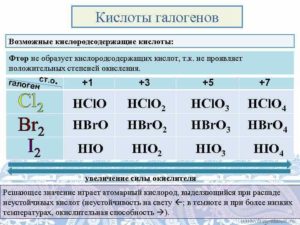
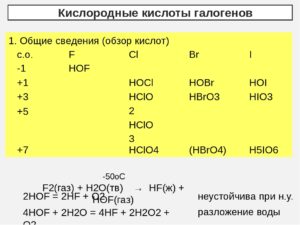
Из учебника химии многие знают, что к галогенам относятся химические элементы периодической системы Менделеева из 17 группы в таблице.
С греческого переводится как рождение, происхождение. Практически все они высокоактивны, благодаря чему бурно реагируют с простыми веществами за исключением нескольких неметаллов. Что же такое галогены и каковы их свойства?
…
- Перечень галогенов
- Фтор
- Хлор
- Бром, йод и астат
- Применение
- Перечень галогенов
- Фтор
- Хлор
- Бром, йод и астат
- Применение
- Гиалуроновая кислота для лица: как применять в домашних условиях и какие процедуры сделать в салоне
- Полезные свойства
- Вредные свойства
- Противопоказания
- Салонные процедуры
- Критерии выбора
- Правила домашнего применения
- Галогеновая кислота от морщин
- Что это такое и чем полезно
- Показания к применению
- Косметологические процедуры с ГК
- От морщин
- Инъекции для губ
- Носогубные складки
- Эффективные средства в домашних условиях
- В капсулах для приема внутрь
- средств
- Галогены: физические свойства, химические свойства. Применение галогенов и их соединений
- Общая характеристика
- Химические элементы
- Периодические свойства в группе галогенов
- 2.3.1. Химические свойства водорода и галогенов
- с металлами
- с неметаллами
- с оксидами металлов
- c оксидами неметаллов
- c кислотами
- c солями
- Химические свойства галогенов
- Взаимодействие галогенов с простыми веществами
- водородом
- фосфором
- серой
- Взаимодействие галогенов с металлами
- Реакции замещения с галогенами
- Взаимодействие галогенов с водой
- Взаимодействие галогенов с растворами щелочей
Перечень галогенов
Галогены являются хорошими окислителями, по этой причине в природе их можно встретить только в каких-либо соединениях. Чем выше порядковый номер, тем химическая активность элементов этой группы меньше. К группе галогенов относятся нижеперечисленные элементы:
- хлор (Cl);
- фтор (F);
- иод (I);
- бром (Br);
- астат (At).
Последний разработан в институте ядерных исследований, который расположен в городе Дубна. Фтор относится к ядовитым газам бледно-жёлтого цвета. Хлор также ядовит. Это газ, имеющий довольно резкий и неприятный запах светло-зелёного цвета.
Бром имеет красно-бурый окрас, это ядовитая жидкость, которая может даже поражать обоняние. Он очень летуч, поэтому его хранят в ампулах. Йод — кристаллическое легко возгоняющееся вещество тёмно-фиолетового цвета.
Астат радиоактивен, цвет кристаллов: чёрный с синевой, период полураспада составляет 8,1 часа.
: ковалентная неполярная связь, примеры из химии.
Фтор
Высокая активность окисления галогенов падает от фтора к иоду.
Самым активным из собратьев является фтор, который имеет свойство вступать в реакцию с любыми металлами, образуя соли, некоторые из них при этом самовоспламеняются, при этом выделяется огромное количество тепла.
Без нагрева этот элемент реагирует почти со всеми неметаллами, реакции сопровождаются выделением некоторого количества теплоты (экзотермические).
С инертными газами фтор вступает во взаимодействие, при этом облучаясь (Хе + F 2 = XeF 2 + 152 кДж). Нагреваясь, фтор влияет на другие галогены, окисляя их. Имеет место формула: Hal 2 + F 2 = 2НalF, где Hal = Cl, Br, I, At, в случае, когда HalF степени окисления хлора, брома, иода и астата равны + 1.
Со сложными веществами фтор также взаимодействует довольно энергично. Следствием является окисление воды. При этом происходит взрывная реакция, которая коротко записывается формулой: 3F 2 + ЗН 2 О = OF 2 ↑ + 4HF + Н 2 О 2.
Хлор
Активность свободного хлора несколько меньше, в сравнении со фтором, но он также имеет хорошую способность вступать в реакцию.
Это может происходить при взаимодействии со многими простыми веществами, за редким исключением в виде кислорода, азота, инертных газов.
Он может бурно реагировать со сложными веществами, создавая реакции замещения, свойство присоединения углеводородов — это тоже присуще хлору. При нагреве происходит вытеснение брома или йода из соединений с водородом или металлами.
Своеобразные отношения у этого элемента с водородом. При комнатной температуре и без попадания света, хлор никак не реагирует на этот газ, но стоит его лишь нагреть или направить свет, произойдёт взрывная цепная реакция. Формула приведена ниже:
Cl 2 + h ν → 2Cl , Cl + Н 2 → HCl + Н , Н + Cl 2 → HCl + Cl , Cl + Н 2 → HCl + Н и т . д .
Фотоны, возбуждаясь, вызывают разложение на атомы молекул Cl 2, при этом возникает цепная реакция, вызывая появление новых частиц, которые инициируют начало следующей стадии. В истории химии это явление было исследовано. Русский химик и лауреат Нобелевской премии Семёнов Н.Н. в 1956 году занимался изучением цепной фотохимической реакции и внёс тем самым большой вклад в науку.
https://www.youtube.com/watch?v=9yJYVzC_TfI
Хлор реагирует со многими сложными веществами, это реакции замещения и присоединения. Он хорошо растворяется в воде.
Cl 2 + Н 2 О = HCl + HClO — 25 кДж.
Со щелочами при нагреве хлор может диспропорционировать.
Бром, йод и астат
Химическая активность брома чуть меньше, чем у вышеназванных фтора или хлора, однако она тоже довольно велика. Бром часто применяют в жидком виде. Он, как и хлор, очень хорошо растворяется в воде. Происходит частичная реакция с ней, позволяющая получать «бромную воду».
Химическая активность йода заметно отличается от остальных представителей этого ряда. Он почти не взаимодействует с неметаллами, а с металлами реакция идёт очень медленно и только при нагреве.
При этом происходит большое поглощение тепла (эндотермическая реакция), которая сильно обратима. К тому же йод нельзя никаким образом растворить в воде, этого не достичь даже при нагреве, поэтому в природе не бывает «йодной воды». Йод можно растворить только в растворе йодида.
При этом образуются комплексные анионы. В медицине такое соединение называется раствором Люголя.
Астат реагирует с металлами и водородом. В ряду галогенов химическая активность уменьшается по направлению от фтора к астату. Каждый галоген в ряду F — At способен вытеснять последующие элементы из соединений с металлами или водородом. Астат — самый пассивный среди этих элементов. Но ему присуще взаимодействие с металлами.
Применение
Химия прочно входит в нашу жизнь, внедряясь во все сферы. Человек научился применять галогены, а также его соединения на своё благо. Биологическое значение галогенов неоспоримо. Области применения их различны:
- медицина;
- фармакология;
- производство различных пластмасс, красителей и т. д.;
- сельское хозяйство.
Из природного соединение криолита, химическая формула которого выглядит следующим образом: Na3AlF6, получают алюминий. Соединения фтора нашли широкое распространение при производстве зубных паст. Фтор, как известно, служит для профилактики кариеса. Спиртовую настойку йода применяют для дезинфекции и обеззараживания ран.
Наиболее широкое применение в нашей жизни нашёл хлор. Область его применения довольно многообразна. Примеры использования:
- Производство пластмасс.
- Получение соляной кислоты.
- Производство синтетического волокна, растворителей, каучуков и др.
- Отбеливание тканей (льняных и хлопчатобумажных), бумаги.
- Обеззараживание питьевой воды. Но всё чаще для этой цели используется озон, так как применение хлора вредно для организма человека.
- Дезинфекция помещений
Нужно помнить, что галогены — очень токсичные вещества. Особенно ярко это свойство выражено у фтора. Галогены могут оказывать удушающее и воздействие на органы дыхания и поражать биологические ткани.
Огромную опасность могут иметь пары хлора, а также аэрозоль фтора, имеющий слабый запах, он может ощутиться при большой концентрации. Человек может получить эффект удушья. При работе с такими соединениями нужно соблюдать меры предосторожности.
Методы производства галогенов сложные и многообразные. В промышленности к этому подходят с определёнными требованиями, соблюдение которых неукоснительно соблюдаются.
Гиалуроновая кислота для лица: как применять в домашних условиях и какие процедуры сделать в салоне
С течением времени кожа теряет упругость, образуя складки, которые мы называем морщинами. Несмотря на то, что возрастные изменения неизбежны, замедлить их развитие всё-таки можно, продлив молодость.
Для этого сегодня широко используется гиалуроновая кислота. По своей природе это вещество является биологическим материалом и содержится в любом человеческом организме. Она продуцируется в жидкостях (слюне, например), клетках кожи, является важным компонентом суставов. Почему косметологи так активно используют её для борьбы с возрастом?
Полезные свойства
Полезные свойства гиалуроновой кислоты были открыты ещё в середине XX века, и с тех пор к этому веществу не ослабевал интерес косметологов.
До сих пор проводятся научные исследования, лабораторные опыты, выясняются тёмные и светлые стороны этого уникального вещества.
И хотя самые важные открытия, возможно, ещё только впереди, на данный момент никто не может оспорить омолаживающее и лифтинговое действие гиалуроната на кожу, который:
- образует тончайшую, но очень прочную защитную плёнку поверх кожи, усиливая её естественное сопротивление любым агрессивным атакам извне;
- поддерживает в клетках уровень увлажнения, при этом не нарушая газообмен в тканях, чем грешат многие другие косметические средства;
- заполняет возрастные и даже мимические морщины, разглаживая их;
- лечит сухой, шелушащийся эпидермис, делая его нежным, мягким и максимально увлажнённым;
- омолаживает кожу после 30 лет, возвращая ей былые упругость и эластичность;
- усиливает действие других активных компонентов, применяемых с ним по соседству в косметических средствах;
- заживляет раны, шрамы, рубцы;
- используется для лечения в самые короткие сроки угрей и прыщей.
Вот чем полезна гиалуроновая кислота для лица в качестве эффективного омолаживающего средства. Её впечатляющее действие на кожу, которой уже коснулись первые возрастные изменения, заставляет сотни женщин обратиться к этому эликсиру молодости и красоты, чтобы вернуть себе свежесть.
https://www.youtube.com/watch?v=NaydAHEAnu0
Однако нужно понимать, что существует и оборотная сторона: данное вещество в косметологии — это польза и вред одновременно. И без учёта последнего можно столкнуться с побочными эффектами и осложнениями, исправить которые будет очень трудно.
По страницам истории. Название гиалуроновой кислоте дали учёные К. Мейер и Дж. Палмер в 1934 году, которые смогли выделить её из стекловидного тела глаза. Они соединили греческое слово hyalos (что значит стекловидный) и уроновую кислоту.
Вредные свойства
Всё чаще современные женщины спрашивают, вредна ли гиалуроновая кислота для лица и в чём именно может проявиться её тёмная сторона. Откуда вообще пошли такие разговоры? Оказывается, в результате некоторых неудачных применений гиалуроната в косметических целях появились отрицательные отзывы. Так в чём же его обвиняют?
- Вызывает аллергические реакции.
- Может спровоцировать сильную отёчность.
- После уколов слишком долго сохраняется гиперемия кожного покрова.
- При частом использовании кожа способна привыкнуть к такому допингу и совсем прекратить выработку собственной кислоты. Так что как только вы перестанете её использовать для подпитки и омоложения, внешний вид эпидермиса заметно ухудшится.
Как видите, вред на самом деле есть, но лишь в том случае, если её неправильно применять. Это часто происходит в домашних условиях с красавицами, которые игнорируют советы профессионалов и считают, что сами всё знают куда лучше их.
В салонах побочные эффекты и осложнения могут возникнуть по двум причинам. Если укол красоты делал неопытный врач или пациентка скрыла от него заболевание, являющееся противопоказанием.
Перспектива. Гиалуроновая кислота активно используется не только в косметологии, но и в медицине. Согласно научным предположениям, сделанным в Хайфском университете (Израиль), именно это вещество может стать основой для создания эффективных противораковых средств.
Противопоказания
Если противопоказания не были своевременно выявлены и укол всё-таки был сделан, действие гиалуроновой кислоты на кожу лица предсказать невозможно. Реакция организма будет зависеть от индивидуальных особенностей, серьёзности и опасности заболевания, а также качества применённого препарата. Нельзя использовать гиалуронат при наличии следующих патологий и состояний:
- проблемы со свёртываемостью крови;
- беременность;
- инфекционные заболевания;
- лактация;
- индивидуальная непереносимость;
- обширные очаги воспаления;
- аутоиммунные заболевания: диабет, артрит;
- недавно проведённые глубокий (химический) пилинг или лазерная шлифовка лица (если прошло менее месяца).
При соблюдении данных противопоказаний эффект будет заметным и ярко выраженным.
Борьба с беспощадным действием времени закончится: морщинки разгладятся, кожа станет по-прежнему упругой, эластичной, посвежевшей, как и несколько лет назад.
От вас будет зависеть лишь выбор, самостоятельно попробовать гиалуронку в составе домашних масок или же воспользоваться услугами современных салонов красоты.
Чудеса природы. 1 молекула гиалуроновой кислоты способна удерживать до 1 000 молекул воды, чем объясняется уникальный увлажняющий эффект этого вещества.
Салонные процедуры
Обратившись в салон красоты с целью омоложения и лифтинга, вы можете рассчитывать на самые разнообразные процедуры, в основе которых будет этот эликсир молодости.
Но для начала проведут небольшое обзорное обследование на наличие противопоказаний, исключат их, подберут самый эффективный в вашем случае метод.
После чего расскажут, как действует гиалуроновая кислота на кожу лица и каких результатов стоит ожидать.
Под кожу инъекционно вводится практически чистая гиалуроновая кислота, а не лечебно-косметический гель с различными примесями.
Используемые в рамках данной процедуры препараты по своему составу очень близки к той гиалуронке, которая до определённого времени продуцируется человеческой кожей.
Такие инъекции заставляют клетки снова синтезировать данное вещество, в результате чего коже возвращаются упругость и эластичность. Одна из самых дорогих, но зато и самых эффективных процедур.
https://www.youtube.com/watch?v=B5ZtzOexfyE
В проблемный участок (носогубные складки, подбородок, щёки) вводится лечебно-косметический гель, заполняющий внутри кожи пустоты, увеличивая объём тканей, активно удерживая влагу внутри клеток. Эффект может сохраняться до 1 года, хотя здесь всё очень индивидуально. Основной недостаток — болезненность инъекций, которая легко устраняется обезболивающими препаратами.
Эффективный способ подкорректировать контуры лица: увеличить губу, сделать скулы более рельефными, убрать второй подбородок, уменьшить глубину морщин или носогубных складок. Используемые в рамках контурной пластики препараты гиалуронки кожа воспринимает как естественный компонент. Эффект сохраняется от полугода.
Любая из этих процедур способна преобразить женщину и подарить ей молодость и красоту. Если всё было сделано профессионально, был использован качественный препарат, вы на собственном опыте узнаете, как гиалуроновая кислота влияет на лицо: увлажняет, омолаживает, регенерирует, подтягивает и позволяет сбросить пару ненавистных лет со своего настоящего возраста.
Однако ни для кого не секрет, что подобные процедуры стоят немалых денег. А что делать тем, у кого их не так много? Ответ очевиден: использовать её в домашних условиях, купив препарат в любой аптеке.
О недостатках. Солнечный ожог на коже есть не что иное, как распад гиалуроновой кислоты под ультрафиолетовыми лучами.
Критерии выбора
На самом деле это вещество можно купить в качестве лекарственного препарата в любой аптеке, так как отпускается оно свободно, без рецепта. Но какую гиалуроновую кислоту выбрать для лица, чтобы она оказалась максимально полезной для косметологических процедур в домашних условиях? Наши советы помогут вам.
- Зная, в чём содержится гиалуроновая кислота, многие женщины отказываются от её использования с эстетической точки зрения. Раньше она производилась из петушиных гребней и глаз крупного рогатого скота. Современные технологии изменились, и теперь это вещество синтезируют в процессе своей жизнедеятельности специальные бактерии. Качество препарата осталось тем же.
- Изучите состав. Лучшим действием на кожу обладает низкомолекулярная гиалуроновая кислота, чем высокомолекулярная, так как она лучше транспортируется через кожный покров, достигая самых глубоких слоёв дермы. Кремы и маски на её основе получаются более приятными, лёгкими и воздушными.
- Любая аптечная продукция сертифицирована, что говорит о её высоком качестве, однако срок годности товара проверять не забывайте.
- Таблетки гиалуроновой кислоты выпускают разные фармацевтические компании. Среди самых востребованных можно отметить следующие:
- Лора от российской компании Эвалар. 36 штук всего за 200 рублей;
- Солгар (Solgar) — американское производство, гиалуроновая кислота дополнена коллагеном, кальцием, хондроитином сульфатом. 30 таблеток обойдутся в 2 000 рублей;
- Doppel Herz — немецкий препарат. В составе значатся ещё и витамины, пантотен, биотин. Стоимость — 500 рублей.
- KWC — японский комплекс из гиалуроновой кислоты, коллагена, коэнзима Q10 и витаминов. 90 капсул стоят 3 000 рублей.
Теперь вы сможете приобрести качественный товар в аптеке совсем по невысокой цене. Но нужно понимать, что такой эффективности от неё, как в салоне, всё равно добиться не удастся. Тем не менее, омолаживающее действие будут оказывать даже самые простые домашние маски, приготовленные на её основе.
Полезный совет. Имейте в виду, что если вы решились сделать себе укол красоты с помощью гиалуроновой кислоты, за неделю до процедуры вам нельзя будет пить алкоголь и зелёный чай.
Правила домашнего применения
Помня о том, что у вас в руках — аптечный, т. е. медицинский препарат, для начала ознакомьтесь с его инструкцией и следуйте ей. А также старайтесь придерживаться следующих советов:
- Объективно оцените, что даёт гиалуроновая кислота для лица на самом деле и насколько это вам необходимо. Её основная функция — омоложение и только потом увлажнение. Поэтому в 20 лет этот препарат можно использовать лишь тем девушкам, которые страдают от сильной сухости кожного покрова и большого количества постоянных шелушений.
- Превратите таблетки в порошок.
- Порошок (2 гр) разведите в кипячёной, но уже остуженной до тёплого состояния воде (не более 30 мл). Перемешайте венчиком, чтобы получился крем, оставьте эту массу набухать на полчаса или даже час. Образовавшиеся комочки разомните: консистенция должна быть однородной и вязкой. Храните этот раствор в замороженном виде не более 2 недель.
- Проверьте, не начнётся ли у вас аллергия: нанесите кислоту на запястье и в течение суток отслеживайте реакцию кожи.
- Приготовленный раствор можно использовать как базу для домашних масок или основу для крема, добавляя к нему дополнительные ингредиенты. Можно в чистом виде наносить на предварительно очищенную кожу.
- Если нужно разгладить морщины на всей поверхности лица, раствор равномерно распределяется по коже. Если хотите только избавиться от прыща, можно использовать его точечно.
- После нанесения образуется приятная гелевая плёнка, которая быстро впитается в кожу. Смывания не потребуется.
- Теперь можно нанести омолаживающий ночной крем (процедуру лучше делать за 1-2 часа до сна).
- Регулярность — 1-2 раза в неделю.
- Домашнее применение гиалуроновой кислоты должно быть в рамках нескольких омолаживающих курсов для достижения большего эффекта. Например, 10-15 масок, а затем — перерыв в 2 недели, и снова — новый курс.
- Летом такие маски лучше не делать, так как ультрафиолет сведёт все ваши усилия к нулю.
Многие современные женщины интересуются, как пользоваться гиалуроновой кислотой для омоложения лица не только в условиях салонов красоты, но и дома. С одной стороны, не нужно тратить большие денежные средства.
С другой стороны, можно полностью довериться опытным рукам профессионалов, которым в любом случае придётся ответить за результат.
Решать только вам, каким именно способом возвратить своей коже молодость с помощью этого удивительного по своим косметическим свойствам вещества.
Галогеновая кислота от морщин
Приветствую вас, дорогие читательницы! А знаете ли вы, что наша кожа стареет из-за потери влаги? Это неизбежно происходит в связи с уменьшением уровня Hyaluronic Acid в верхних слоях дермы. Уже после 30 лет количество этого вещества в организме начинает заметно сокращаться. Давайте разберемся, чем полезна гиалуроновая кислота для лица и как ее можно восстановить.
Что это такое и чем полезно
Сегодня Hyaluronic Acid — самый популярный ингредиент в антивозрастной уходовой косметике. Это вещество, которое содержится в теле человека в составе эпителиальной, соединительной, нервной тканей. Наряду с коллагеном и эластином она является важнейшей составляющей внутриклеточного матрикса кожи.
Самое главное свойство Hyaluronic Acid – это ее способность связывать воду. 1 молекула ГК связывает 1000 молекул воды
Действует простой принцип: чем больше гиалуроновой кислоты (ГК), тем свежее и эластичнее наша кожа. А значит, тем моложе мы выглядим! Именно поэтому гиалуронка так эффективна в увлажняющих средствах. А глубокое увлажнение – это главное, что необходимо для антивозрастной косметики.
https://www.youtube.com/watch?v=ZFtI0GjM9d8
Благодаря способности аккумулировать влагу, Hyaluronic Acid выполняет следующие функции:
- транспортирует воду;
- стабилизирует водный баланс в коже;
- повышает синтез коллагена и эластина;
- придает упругость тканям;
- нейтрализует свободные радикалы.
ГК применяемая в косметике, бывает двух видов – высокомолекулярная и низкомолекулярная. Какая лучше? Обе. Применяются они для разных целей.
Высокомолекулярная ГК (с крупным размером молекулы) очень мало впитывается кожей. Зато она создает на поверхности эпидермиса своеобразный защитный слой. Он не позволяет влаге испаряться с поверхности кожи. Одновременно эта тончайшая пленка препятствует агрессивным воздействиям извне. Что особенно важно – этот барьер газопроницаемый. Так что кожа нормально «дышит» под ним.
Низкомолекулярная ГК имеет размер меньше 5 нм в диаметре. Проникает вглубь кожи, увлажняет ее изнутри. Она же помогает впитываться другим полезным ингредиентам косметики.
Посмотрите видео-отзыв косметолога с подробным разбором «что такое гиалуронка»:
Показания к применению
До 25-30 лет организм самостоятельно вырабатывает гиалуронку в достаточных количествах. Однако с возрастом ее синтез снижается, в результате кожа становится сухой, тонкой, теряет эластичность и тургор.
Прямые показания к применению ГК:
- возрастные изменения, морщины;
- тонкая чувствительная кожа;
- сухая, шелушащаяся кожа;
- потеря тонуса и эластичности;
- рубцы, шрамы, постакне.
Сейчас гиалуронат применяется также для коррекции внешности – уменьшение носогубных складок, увеличение губ и т.п. Процедуры переносятся хорошо и очень редко вызывают аллергическую реакцию. Эффект длится примерно 1-1,5 года. Заметный результат отмечается в возрасте 30-40 лет, когда выработка собственной гиалуронки начинает падать.
Гиалуронка или ботокс – что лучше? В некоторых случаях уколы гиалуроновой кислоты могут быть уже неэффективны. Это возможно при очень глубоких морщинах, сильных возрастных изменениях.
Но надо понимать, что ботокс – это токсичное вещество. По сути, оно разглаживает морщины, блокируя нервные импульсы. Он, как декоративная косметика, дает видимый эффект на некоторое время.
В чем плюс и минус этого препарата я описала в статье «как действует ботокс для лица».
Косметологические процедуры с ГК
Своевременный поход к косметологу может значительно отодвинуть необходимость таких серьезных вмешательств, как контурная пластика лица и подтяжка. В косметологии ГК применяется для проведения множества различных аппаратных и инъекционных процедур. Посмотрите сами, фото до и после свидетельствуют об их результативности.
От морщин
В числе эффективных процедур для лица с применением гиалуроновой кислоты можно выделить мезотерапию, биоармирование и биоревитализацию, а также инъекции. Косметолог может предложить разные способы воздействия. У каждого из них есть свои плюсы и минусы.
Все эти процедуры основаны на введении гиалуроновой кислоты в глубокие слои кожи. Такие методики позволяют избавиться от морщин, подтянуть овал лица, очертить скулы
Так, при фракционной мезотерапии на коже делается множество микропроколов. По получившимся микроканалам средство проникает вглубь кожи. При биоармировании филлеры на основе гиалуронки вводятся по определенным линиям, формирующим контуры лица. При ревитализации средство может вводиться с помощью лазера.
Для век и области вокруг глаз и носа используются самые щадящие методы. Так, при мезотерапии выбираются иглы длиной не более 0,25 мм. Какая процедура вам избавиться от темных кругов под глазами, смотрите в другой статье.
Инъекции для губ
Гиалуроновая кислота также используется для коррекции формы и увеличения объема губ. Это значительно более безопасно, чем использование каких бы то ни было других наполнителей. В отличие от силикона, гиалуронка – вещество, которое в нашем организме уже содержится.
https://www.youtube.com/watch?v=u8rlVBR9rN8
В первые дни после коррекции возможна отечность, припухлость, покраснение кожи вокруг губ. Эти симптомы вскоре проходят. В первую неделю нельзя посещать бассейн, сауну, баню или солярий.
Эффект от инъекций гиалуронкой на губах держится не слишком долго. Максимальная длительность – до полугода. Для действительно долгосрочного эффекта применяются синтетические наполнители на основе силикона.
Носогубные складки
Для воздействия на носогубные складки чаще всего применяются инъекции с филлерами на основе гиалуроновой кислоты. Он заполняет складку и как бы выталкивает ее изнутри.
Сразу после инъекций на коже может образоваться небольшая бугристость. Это нормально и проходит обычно в течение двух-трех дней.
Чистая гиалуронка дает самую большую бугристость, зато и омолаживающий эффект от нее самый заметный. Препараты с витаминными коктейлями позволяют свести к минимуму негативный эффект первых дней.
Подходящий препарат в каждом конкретном случае должен подбирать врач-косметолог.
Уже на следующий день после процедуры можно начинать пользоваться привычными уходовыми косметическими средствами для своего типа кожи. Эффект от такой процедуры держится обычно от 6 месяцев до 2-х лет. Согласитесь, это вполне длительный срок.
Эффективные средства в домашних условиях
Самые распространенные и знакомые всем средства домашнего ухода за лицом – это крема, маски и сыворотки. Рекомендации косметологов и отзывы потребителей свидетельствуют об эффективности таких продуктов.
Для сухой, обезвоженной кожи эти средства подходят в любое время года. При жирной и комбинированной лучше пользоваться осенью и зимой
Крема — добавление гиалуроновой кислоты в его состав позволяет другим активам лучше проникать в кожу. Также гиалуронка создает защитный барьер на дерме. Идеально подходят уходовые средства с ГК для чувствительной тонкой кожи вокруг глаз. Она нуждается в глубоком увлажнении и в то же время ее нельзя утяжелять.
Сыворотки – в отличие от крема, они не содержат жиров. За счет этого в них увеличена концентрация водорастворимых активов. Сыворотки на водной основе наносятся на кожу после умывания пенкой и до применения крема. Другой вариант – добавить каплю непосредственно в крем. Назначение таких сывороток именно в том, чтобы улучшить впитываемость крема и усилить его действие.
Маски — концентрация активных ингредиентов в этих продуктах увеличена еще больше. Маска наносится толстым слоем или на салфетки.
В течение периода активного действия она постоянно остается влажной. Маски прицельно воздействуют на проблему — дают глубокое увлажнение, омолаживают и восстанавливают кожу.
В статье «рейтинг увлажняющих масок для лица» я сделала подборку хороших уходовых средств.
В аптеке можно приобрести сухой гиалуронат натрия. Вообще-то назначение этого средства вовсе не косметическое. Оно необходимо для диагностических операций в офтальмологии. Но многие женщины используют этот порошок для домашних косметических процедур.
Для этого готовят раствор 2 г кислоты на 30 мл теплой кипяченой воды. Смесь тщательно перемешивают и дают постоять около двух часов. В готовом растворе не должно быть комков. Наносят на очищенную кожу перед нанесением крема или маски. Курс составляет 10-15 применений.
В капсулах для приема внутрь
Наиболее эффективно воздействовать на кожу одновременно снаружи и изнутри. Именно для этой цели существуют капсулы с гиалуроновой кислотой, которые можно приобрести на Айхербе .
Сфера применения ГК – улучшение состояния кожи, ногтей, волос. В идеале стоит сочетать прием гиалуронки и коллагена I и III типа. В этом случае улучшение состояния кожи буквально налицо
Прием гиалуронки внутрь поможет решить и проблемы с суставами и связками. Она полезна также для костей и сухожилий. В этих целях ГК, оптимально будет сочетать с коллагеном II типа, глюкозамином и хондроитином.
https://www.youtube.com/watch?v=F_E_wMRF354
При приеме гиалуроновой кислоты внутрь обязательно нужно увеличивать потребление жидкости. Нужно выпивать не менее двух литров чистой воды в день. В противном случае возможны побочные эффекты запоры, тошнота, сухость кожи и прочее. Самый распространенный побочный эффект – это высокая отечность. Если она появилась, необходимо увеличить потребление чистой воды.
средств
Многие бренды сегодня производят целые линейки средств с гиалуроновой кислотой. Цена варьируется в очень широком диапазоне – от масс-маркета до элитных серий. Расскажу о некоторых средствах, которые по отзывам хорошо себя зарекомендовали.
Либридерм – увлажняющая серия из дневного, ночного средства и крема вокруг глаз. Подходит для всех типов кожи, особенно полезно чувствительной, склонной к сухости. Питает и смягчает, содержит все необходимые ингредиенты для восстановления кожного барьера. Без отдушек и других раздражителей. Можно купить в аптеке.
В линейке Hyaluronic от Либоридерм есть еще замечательные средства для комплексного ухода: сыворотка, тоник, вода и другие.
AquaBaseотNovosvit – это праймер от глубоких морщин, обладающий глубоким увлажняющим и выравнивающим эффектом.
Идеален для кожи, склонной к жирности и неровностям на лице. Легкая текстура, средней густоты, впитывается быстро. По отзывам ложится на кожу хорошо и не скатывается.
Радует, что Sodium Hyaluronate стоит третьим в списке ингредиентов.
Галогены: физические свойства, химические свойства. Применение галогенов и их соединений
Галогены в периодической таблице расположены слева от благородных газов. Эти пять токсических неметаллических элементов входят в 7 группу периодической таблицы. К ним относятся фтор, хлор, бром, йод и астат.
Хотя астат радиоактивен и имеет только короткоживущие изотопы, он ведет себя, как йод, и его часто причисляют к галогенам. Поскольку галогенные элементы имеют семь валентных электронов, им необходим лишь один дополнительный электрон для образования полного октета.
Эта характеристика делает их более активными, чем другие группы неметаллов.
Общая характеристика
Галогены образуют двухатомные молекулы (вида Х2, где Х обозначает атом галогена) – устойчивую форму существования галогенов в виде свободных элементов.
Связи этих двухатомных молекул являются неполярными, ковалентными и одинарными.
Химические свойства галогенов позволяют им легко вступать в соединение с большинством элементов, поэтому они никогда не встречаются в несвязанном виде в природе. Фтор – наиболее активный галоген, а астат – наименее.
Все галогены образуют соли I группы с похожими свойствами. В этих соединениях галогены присутствуют в виде галоидных анионов с зарядом -1 (например, Cl-, Br-). Окончание -ид указывает на наличие галогенид-анионов; например Cl- называется «хлорид».
Кроме того, химические свойства галогенов позволяют им действовать в качестве окислителей – окислять металлы. Большинство химических реакций, в которых участвуют галогены – окислительно-восстановительные в водном растворе.
Галогены образуют одинарные связи с углеродом или азотом в органических соединениях, где степень их окисления (СО) равна -1. Когда атом галогена замещён ковалентно-связанным атомом водорода в органическом соединении, префикс гало- может быть использован в общем смысле, или префиксы фтор-, хлор-, бром- , йод- – для конкретных галогенов.
Галогенные элементы могут иметь перекрёстную связь с образованием двухатомных молекул с полярными ковалентными одинарными связями.
Хлор (Cl2) стал первым галогеном, открытым в 1774 г., затем были открыты йод (I2), бром (Br2), фтор (F2) и астат (At, обнаружен последним, в 1940 г.). Название «галоген» происходит от греческих корней hal- («соль») и -gen («образовывать»).
Вместе эти слова означают «солеобразующий», подчёркивая тот факт, что галогены, вступая в реакцию с металлами, образуют соли. Галит – это название каменной соли, природного минерала, состоящего из хлорида натрия (NaCl).
И, наконец, галогены используются в быту – фторид содержится в зубной пасте, хлор обеззараживает питьевую воду, а йод содействует выработке гормонов щитовидной железы.
Химические элементы
Фтор – элемент с атомным номером 9, обозначается символом F. Элементарный фтор впервые был обнаружен в 1886 г. путем выделения его из плавиковой кислоты. В свободном состоянии фтор существует в виде двухатомной молекулы (F2) и является наиболее распространенным галогеном в земной коре. Фтор – наиболее электроотрицательный элемент в периодической таблице.
При комнатной температуре является бледно-жёлтым газом. Фтор также имеет относительно небольшой атомный радиус. Его СО – -1, за исключением элементарного двухатомного состояния, в котором его степень окисления равна нулю. Фтор чрезвычайно химически активен и непосредственно взаимодействует со всеми элементами, кроме гелия (He), неона (Ne) и аргона (Ar).
В растворе H2O, плавиковой кислоты (HF) является слабой кислотой. Хотя фтор сильно электроотрицателен, его электроотрицательность не определяет кислотность; HF является слабой кислотой в связи с тем, что ион фтора основной (рН> 7). Кроме того, фтор производит очень мощные окислители.
Например, фтор может вступать в реакцию с инертным газом ксеноном и образует сильный окислитель дифторид ксенона (XeF2). У фтора множество применений.
https://www.youtube.com/watch?v=UGM7PlvtNGQ
Хлор – элемент с атомным номером 17 и химическим символом Cl. Обнаружен в 1774 г. путём выделения его из соляной кислоты. В своём элементарном состоянии он образует двухатомную молекулу Cl2. Хлор имеет несколько СО: -1, +1, 3, 5 и 7. При комнатной температуре он является светло-зеленым газом.
Так как связь, которая образуется между двумя атомами хлора, является слабой, молекула Cl2 обладает очень высокой способностью вступать в соединения. Хлор реагирует с металлами с образованием солей, которые называются хлориды. Ионы хлора являются наиболее распространенными ионами, они содержатся в морской воде. Хлор также имеет два изотопа: 35Cl и 37Cl.
Хлорид натрия является наиболее распространенным соединением из всех хлоридов.
Бром – химический элемент с атомным номером 35 и символом Br. Впервые был обнаружен в 1826 г. В элементарной форме бром является двухатомной молекулой Br2. При комнатной температуре представляет собой красновато-коричневую жидкость. Его СО – -1, + 1, 3, 4 и 5.
Бром более активен, чем йод, но менее активен, чем хлор. Кроме того, бром имеет два изотопа: 79Вг и 81Вг. Бром встречается в виде солей бромида, растворённых в морской воде. За последние годы производство бромида в мире значительно увеличилось благодаря его доступности и продолжительному времени жизни.
Как и другие галогены, бром является окислителем и очень токсичен.
Йод – химический элемент с атомным номером 53 и символом I. Йод имеет степени окисления: -1, +1, +5 и +7. Существует в виде двухатомной молекулы, I2. При комнатной температуре является твёрдым веществом фиолетового цвета. Йод имеет один стабильный изотоп — 127I. Впервые обнаружен в 1811 г.
с помощью морских водорослей и серной кислоты. В настоящее время ионы йода, могут быть выделены в морской воде. Несмотря на то что йод не очень хорошо растворим в воде, его растворимость может возрасти при использовании отдельных йодидов.
Йод играет важную роль в организме, участвуя в выработке гормонов щитовидной железы.
Астат – радиоактивный элемент с атомным номером 85 и символом At. Его возможные степени окисления: -1, +1, 3, 5 и 7. Единственный галоген, не являющийся двухатомной молекулой. В нормальных условиях является металлическим твёрдым веществом чёрного цвета.
Астат является очень редким элементом, поэтому о нём известно немного. Кроме того, астат имеет очень короткий период полураспада, не дольше нескольких часов. Получен в 1940 г. в результате синтеза. Полагают, что астат похож на йод.
Отличается металлическими свойствами.
В таблице ниже показано строение атомов галогенов, структура внешнего слоя электронов.
| Галоген | Конфигурация электронов |
| Фтор | 1s2 2s2 2p5 |
| Хлор | 3s2 3p5 |
| Бром | 3d10 4s2 4p5 |
| Иод | 4d10 5s2 5p5 |
| Астат | 4f14 5d10 6s2 6p5 |
Подобное строение внешнего слоя электронов обусловливает то, что физические и химические свойства галогенов похожи. Вместе с тем при сопоставлении этих элементов наблюдаются и различия.
Периодические свойства в группе галогенов
Физические свойства простых веществ галогенов изменяются с повышением порядкового номера элемента. Для лучшего усвоения и большей наглядности мы предлагаем вам несколько таблиц.
Точки плавления и кипения в группе возрастают по мере роста размера молекулы (F
2.3.1. Химические свойства водорода и галогенов
Атом водорода имеет электронную формулу внешнего (и единственного) электронного уровня 1s1. С одной стороны, по наличию одного электрона на внешнем электронном уровне атом водорода похож на атомы щелочных металлов.
Однако, ему, так же как и галогенам не хватает до заполнения внешнего электронного уровня всего одного электрона, поскольку на первом электронном уровне может располагаться не более 2-х электронов.
Выходит, что водород можно поместить одновременно как в первую, так и в предпоследнюю (седьмую) группу таблицы Менделеева, что иногда и делается в различных вариантах периодической системы:
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (H2).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
с металлами
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н2 является окислителем.
с неметаллами
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
https://www.youtube.com/watch?v=UAqivFHR-7M
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
с оксидами металлов
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
c оксидами неметаллов
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
Смесь CO и H2 даже имеет свое собственное название – «синтез-газ», поскольку из нее в зависимости от условий могут быть получены такие востребованные продукты промышленности как метанол, формальдегид и даже синтетические углеводороды:
c кислотами
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
c солями
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Химические свойства галогенов
Галогенами называют химические элементы VIIA группы (F, Cl, Br, I, At), а также образуемые ими простые вещества. Здесь и далее по тексту, если не сказано иное, под галогенами будут пониматься именно простые вещества.
Все галогены имеют молекулярное строение, что обусловливает низкие температуры плавления и кипения данных веществ. Молекулы галогенов двухатомны, т.е. их формулу можно записать в общем виде как Hal2.
| F2 | Светло-желтый газ с резким раздражающим запахом |
| Cl2 | Желто-зеленый газ с резким удушливым запахом |
| Br2 | Красно-бурая жидкость с резким зловонным запахом |
| I2 | Твердое вещество с резким запахом, образующее черно-фиолетовые кристаллы |
Следует отметить такое специфическое физическое свойство йода, как его способность к сублимации или, иначе говоря, возгонке. Возгонкой, называют явление, при котором вещество, находящееся в твердом состоянии, при нагревании не плавится, а, минуя жидкую фазу, сразу же переходит в газообразное состояние.
Электронное строение внешнего энергетического уровня атома любого галогена имеет вид ns2np5, где n – номер периода таблицы Менделеева, в котором расположен галоген.
Как можно заметить, до восьмиэлектронной внешней оболочки атомам галогенов не хватает всего одного электрона. Из этого логично предположить преимущественно окисляющие свойства свободных галогенов, что подтверждается и на практике.
Как известно, электроотрицательность неметаллов при движении вниз по подгруппе снижается, в связи с чем активность галогенов уменьшается в ряду:
F2 > Cl2 > Br2 > I2
Взаимодействие галогенов с простыми веществами
Все галогены являются высокоактивными веществами и реагируют с большинством простых веществ.
Однако, следует отметить, что фтор из-за своей чрезвычайно высокой реакционной способности может реагировать даже с теми простыми веществами, с которыми не могут реагировать остальные галогены.
К таким простым веществам относятся кислород, углерод (алмаз), азот, платина, золото и некоторые благородные газы (ксенон и криптон). Т.е. фактически, фтор не реагирует лишь с некоторыми благородными газами.
Остальные галогены, т.е. хлор, бром и йод, также являются активными веществами, однако менее активными, чем фтор. Они реагируют практически со всеми простыми веществами, кроме кислорода, азота, углерода в виде алмаза, платины, золота и благородных газов.
водородом
При взаимодействии всех галогенов с водородом образуются галогеноводороды с общей формулой HHal. При этом, реакция фтора с водородом начинается самопроизвольно даже в темноте и протекает со взрывом в соответствии с уравнением:
Реакция хлора с водородом может быть инициирована интенсивным ультрафиолетовым облучением или нагреванием. Также протекает со взрывом:
Бром и йод реагируют с водородом только при нагревании и при этом, реакция с йодом является обратимой:
фосфором
Взаимодействие фтора с фосфором приводит к окислению фосфора до высшей степени окисления (+5). При этом происходит образование пентафторида фосфора:
При взаимодействии хлора и брома с фосфором возможно получение галогенидов фосфора как в степени окисления + 3, так и в степени окисления +5, что зависит от пропорций реагирующих веществ:
При этом в случае белого фосфора в атмосфере фтора, хлора или жидком броме реакция начинается самопроизвольно.
https://www.youtube.com/watch?v=ozpPfghyIfs
Взаимодействие же фосфора с йодом может привести к образованию только триодида фосфора из-за существенно меньшей, чем у остальных галогенов окисляющей способности:
серой
Фтор окисляет серу до высшей степени окисления +6, образуя гексафторид серы:
Хлор и бром реагируют с серой, образуя соединения, содержащие серу в крайне не свойственных ей степенях окисления +1 и +2. Данные взаимодействия являются весьма специфичными, и для сдачи ЕГЭ по химии умение записывать уравнения этих взаимодействий не обязательно. Поэтому три нижеследующих уравнения даны скорее для ознакомления:
Взаимодействие галогенов с металлами
Как уже было сказано выше, фтор способен реагировать со всеми металлами, даже такими малоактивными как платина и золото:
Остальные галогены реагируют со всеми металлами кроме платины и золота:
Реакции замещения с галогенами
Более активные галогены, т.е. химические элементы которых расположены выше в таблице Менделеева, способны вытеснять менее активные галогены из образуемых ими галогеноводородных кислот и галогенидов металлов:
Аналогичным образом, бром и йод вытесняют серу из растворов сульфидов и или сероводорода:
Хлор является более сильным окислителем и окисляет сероводород в его водном растворе не до серы, а до серной кислоты:
Взаимодействие галогенов с водой
Вода горит во фторе синим пламенем в соответствии с уравнением реакции:
Бром и хлор реагируют с водой иначе, чем фтор. Если фтор выступал в роли окислителя, то хлор и бром диспропорционируют в воде, образуя смесь кислот. При этом реакции обратимы:
Взаимодействие йода с водой протекает в настолько ничтожно малой степени, что им можно пренебречь и считать, что реакция не протекает вовсе.
Взаимодействие галогенов с растворами щелочей
Фтор при взаимодействии с водным раствором щелочи опять же выступает в роли окислителя:
Умение записывать данное уравнение не требуется для сдачи ЕГЭ. Достаточно знать факт о возможности такого взаимодействия и окислительной роли фтора в этой реакции.
В отличие от фтора, остальные галогены в растворах щелочей диспропорционируют, то есть одновременно и повышают и понижают свою степень окисления. При этом, в случае хлора и брома в зависимости от температуры возможно протекание по двум разным направлениям. В частности, на холоду реакции протекают следующим образом:
а при нагревании:
Йод реагирует с щелочами исключительно по второму варианту, т.е. с образованием йодата, т.к. гипоиодит не устойчив не только при нагревании, но также при обычной температуре и даже на холоду: